
Содержание
- Когда применяются СО предприятия?
- СО для качественного анализа
- СО основного вещества для количественного анализа
- СО примесей
- Оценивавшие неопределенности аттестованного значения
- Аттестация, оценка однородности и стабильности, упаковка, маркировка и хранение
- Где взять материал для изготовления СО?
- Где проводить аттестацию?
- Консультация по аттестации СО предприятия
- Литература
Когда применяются СО предприятия?
Стандартные образцы используются при анализе большинства лекарственных средств
В качестве СО при анализе фарм. субстанций следует использовать фармакопейные стандартные образцы, аттестованные уполномоченным фармакопейным органом
На практике, т.к. отечественных фармакопейных СО пока нет, используются стандартные образцы европейской (EP) и американской (USP) фармакопей.
Для некоторых субстанций стандартных образцов, аттестованных уполномоченным фармакопейным органом, просто не существует. Например, если предприятие выпускает новую или редкую субстанцию.
В этом случае предприятия-производители разрабатывают и аттестуют собственные первичные СО, в форме стандартного образца предприятия (СОП):
При их [CО, аттестованных уполномоченным фармакопейным органом] отсутствии для идентификации и оценки содержания действующего вещества должны использоваться первичные стандартные образцы
В ГФ XIV вошла новая фармакопейная статья, посвященная разработке и аттестации стандартных образцов: ОФС.1.1.0007.18 "Стандартные образцы".
Подробно о стандартных образцах
первичные и вторичные СО, RM, CRM, ГСО, международные СО, СО предприятия, фармацевтические СО
Предприятия так же могут использовать вторичные СО предприятия в рутинном анализе, для снижения расхода дорогостоящих фармакопейных СО.
СО для качественного анализа
Назначение CО для качественного анализа
СО основного вещества применяются:
- при подтверждении подлинности фарм. субстанций как образец сравнения (ВЭЖХ, ИК, УФ)
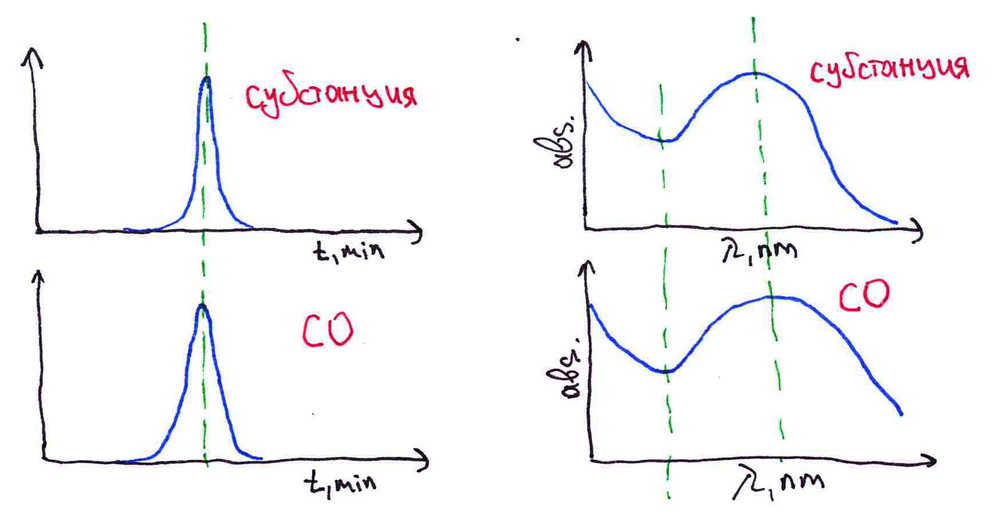
- при определении подлинности действующего вещества в препарате (ВЭЖХ)
СО примесей применяются (ВЭЖХ):
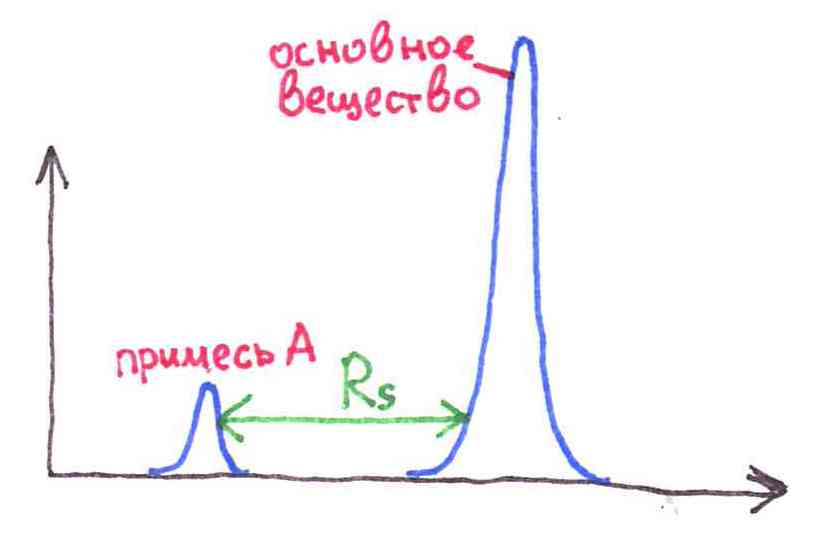
- для проверки разрешающей способности хроматографической системы (разрешения) при анализе субстанций и препаратов
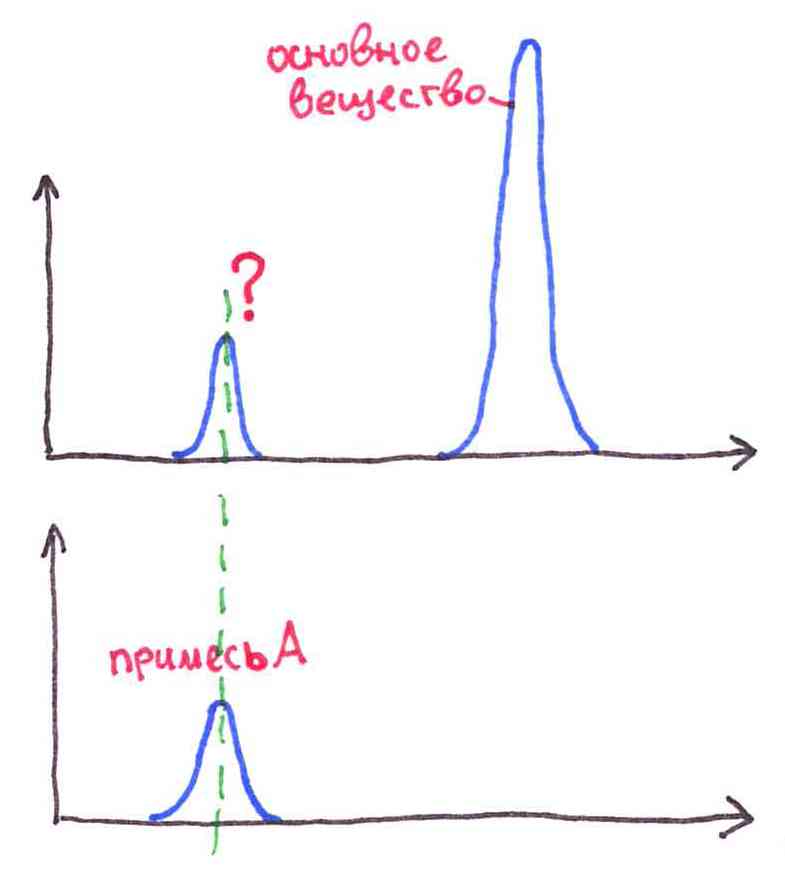
- для подтверждения селективности методики при валидации
- для идентификация примесей в субстанции и препарате (по времени удерживания)
Установление аттестованного значения для первичных СО
Аттестуемый показатель СО для качественного анализа - подлинность (структура)
Для аттестации подлинности (структуры) первичного (primary) стандартного образца должны применяться первичные аналитические методы: спектроскопия ЯМР и масс-спектрометрия.
Масс-спектрометрия
Для анализа органических соединений применяют масс-спектрометры, работающие совместно с газовым или жидкостным хроматографом. Выбор между газовой и жидкостной хромато-масс-спектрометрией определяется свойствами соединения.
Нелетучие и термически-нестабильные соединения анализируют методом жидкостной хромато-масс-спеткрометрии:
 Жидкостной квадруполь-времяпролетный масс-спектрометр Agilent 6550, совмещенный с ВЭЖХ Agilent 1260
Жидкостной квадруполь-времяпролетный масс-спектрометр Agilent 6550, совмещенный с ВЭЖХ Agilent 1260
Записывают хроматограмму и снимают масс-спектр пика основного вещества:
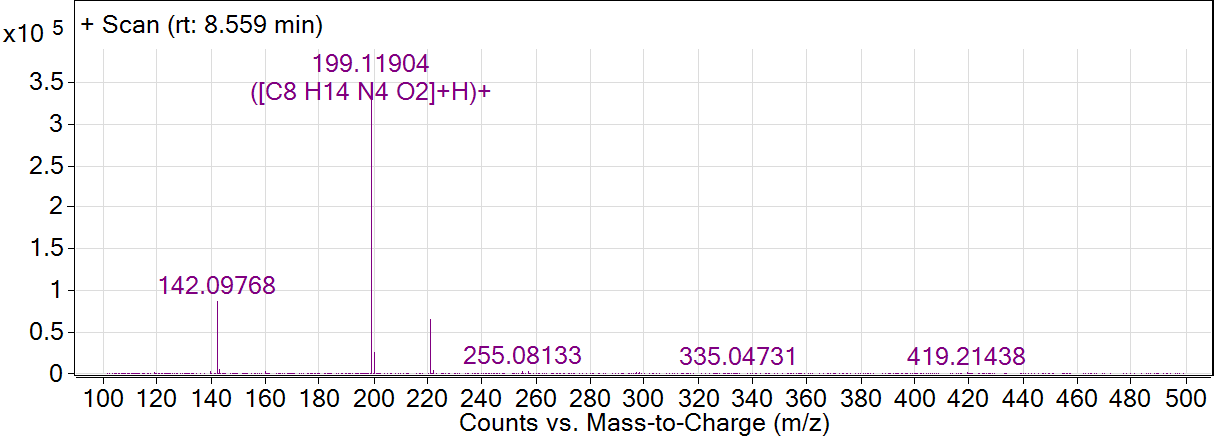 Масс-спектр пика основного вещества
Масс-спектр пика основного вещества
Ионизация в современных жидкостных масс-спектрометрах чаще всего проводится методом электроспрея (ESI). Это "щадящая" ионизация и обычно самый интенсивный пик на масс-спектре соответствен молекулярному иону. Т.е. по масс-спектру в первую очередь устанавливают молекулярную массу соединения, что позволяет подтвердить брутто-формулу.
Из масс-спектра видно, что молекулярный ион имеет отношение массы к заряду m/z = 199.11904 (M+H)+, что соответствует брутто-формуле соединения С8N4O2H14
Летучие и термически-стабильные соединения анализируют методом газовой хромато-масс-спектрометрии:
 Газовый хромато-масс-спектрометр Shimadzu QP-2020
Газовый хромато-масс-спектрометр Shimadzu QP-2020
Ионизация в ГХ-МС в основном осуществляется электронным ударом (EI) - образуются положительно заряженные ионы. Т.к. энергия ионизации высокая (обычно 70 eV), то многие органические соединения под действием электронного пучка просто "разваливаются", т.е. на масс-спектре молекулярный ион не всегда самый интенсивный.
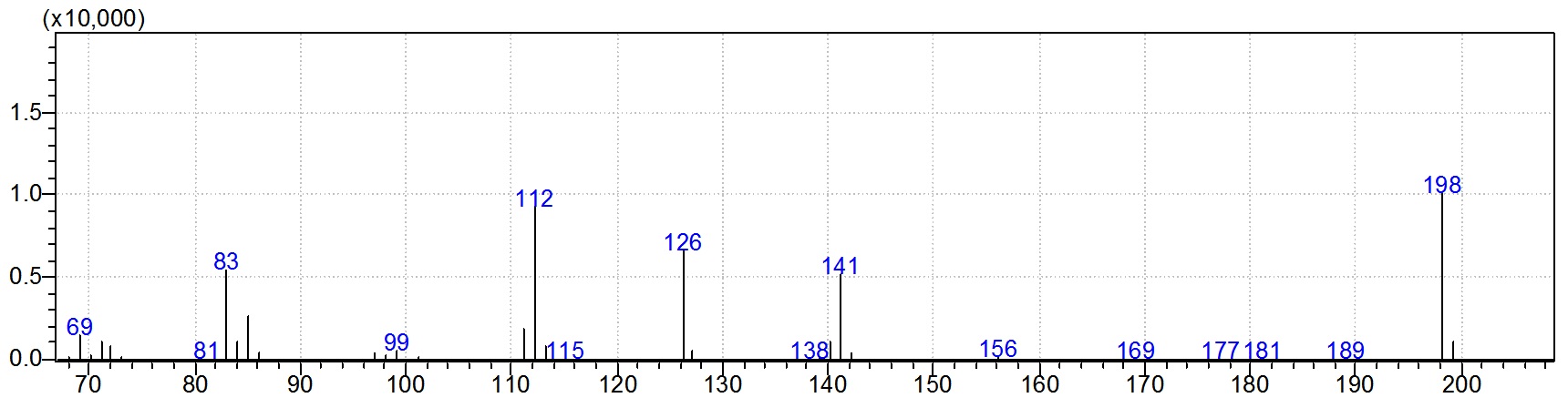 Масс-спектр, полученный на ГХ-МС (ионизация электронным ударом)
Масс-спектр, полученный на ГХ-МС (ионизация электронным ударом)
Идентификация может быть проведена по совпадению масс-спектра с "библиотечным" масс-спектром, содержащихся в базах спектральных данных - Wiley или NIST.
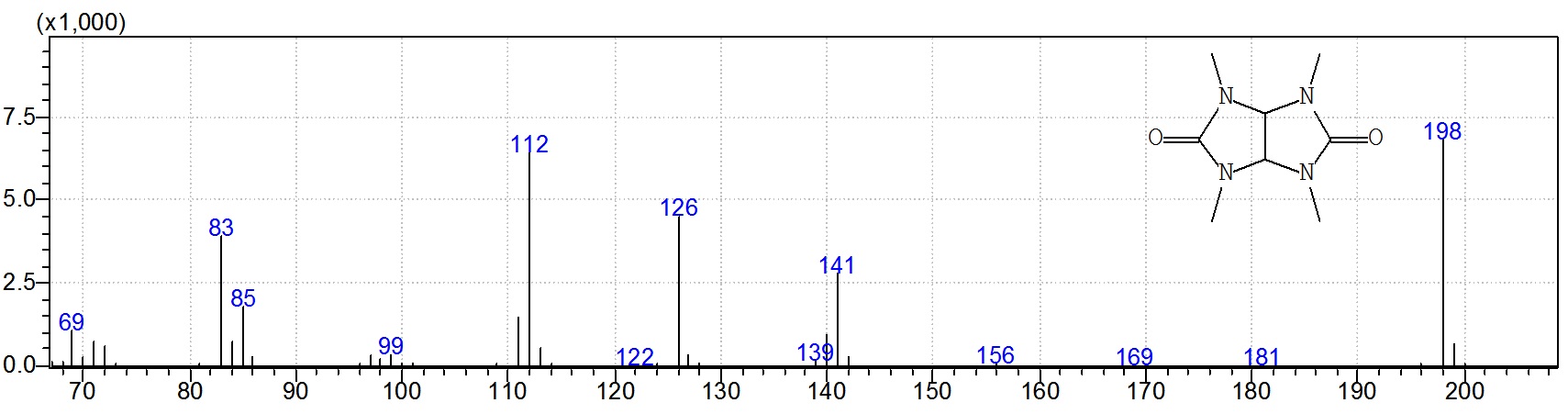 Библиотечный масс-спектр тетраметил-гликолурила (база NITS 14)
Библиотечный масс-спектр тетраметил-гликолурила (база NITS 14)
ЯМР-спектроскопия
Спектроскопия ЯМР - основной метод подтверждения (установления) структуры соединений. Исследование обычно начинают с 1H-спектров.
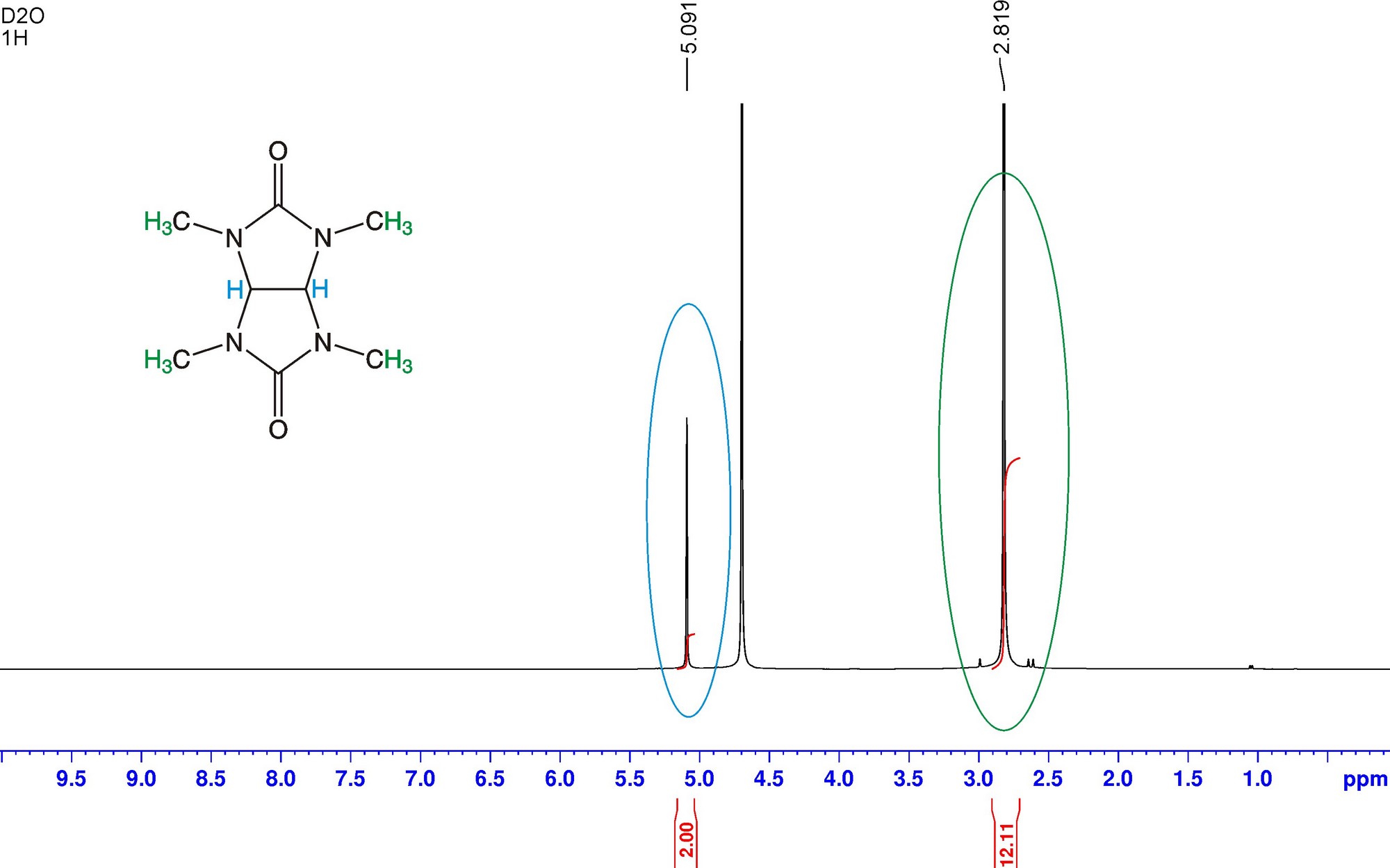 1H-ЯМР-спектр тетраметилгликолурила
1H-ЯМР-спектр тетраметилгликолурила
На спектре наблюдается два синглетных сигнала протонов. Синглет при 2.82 ppm интегральной интенсивностью 12H соответствует 12 эквивалентным протонам четырех -CH3 групп. Синглет при 5.09 ppm интегральной интенсивностью 2H соответствен 2-м эквивалентным протонам "мостиковых" -CH групп.
 13С-ЯМР-спектр тетраметилгликолурила
13С-ЯМР-спектр тетраметилгликолурила
На 13С спектре наблюдается три сигнала. Сигнал при 29.79 ppm соответствует атомам углерода CH3-групп. Сигнал с большим хим. сдвигом - 72.77 ppm соответствует третичным атомам углерода мостиковых CH-групп. Сигнал в области 160 ppm соответствует атомам углерода, связанными с кислородом.
Для сложных соединений не всегда удается полностью "расшифровать" ЯМР-спектр. Однако, связка "ЯМР + масс-спектрометрия" считается золотым стандартом для установления структуры органических соединений.
Дополнительные показатели
Аттестовать образцы для качественного анализа (идентификации) по показателю "массовая доля основного вещества" не требуется. Однако, в качестве дополнительных показателей часто приводят:
- хроматографическую чистоту
- потерю массы при высушивании (влажность)
Дополнительным подтверждением брутто-формулы может служить элементный анализ (массовая доля C,H,N,S), однако на практике (при наличии ЯМР и масс-спектрометрии), по нашему мнению большого смысла делать CHNS-анализ не имеет.
Пример спецификации
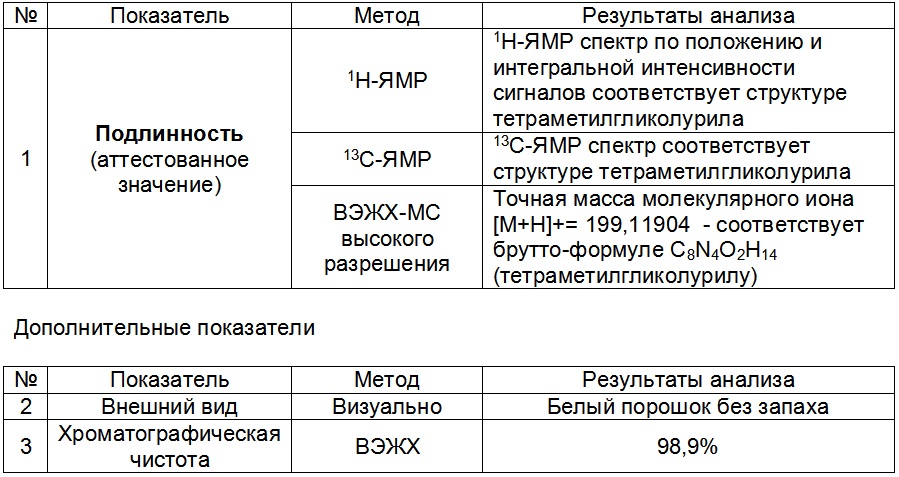
Установление аттестованного значения для вторичных СО
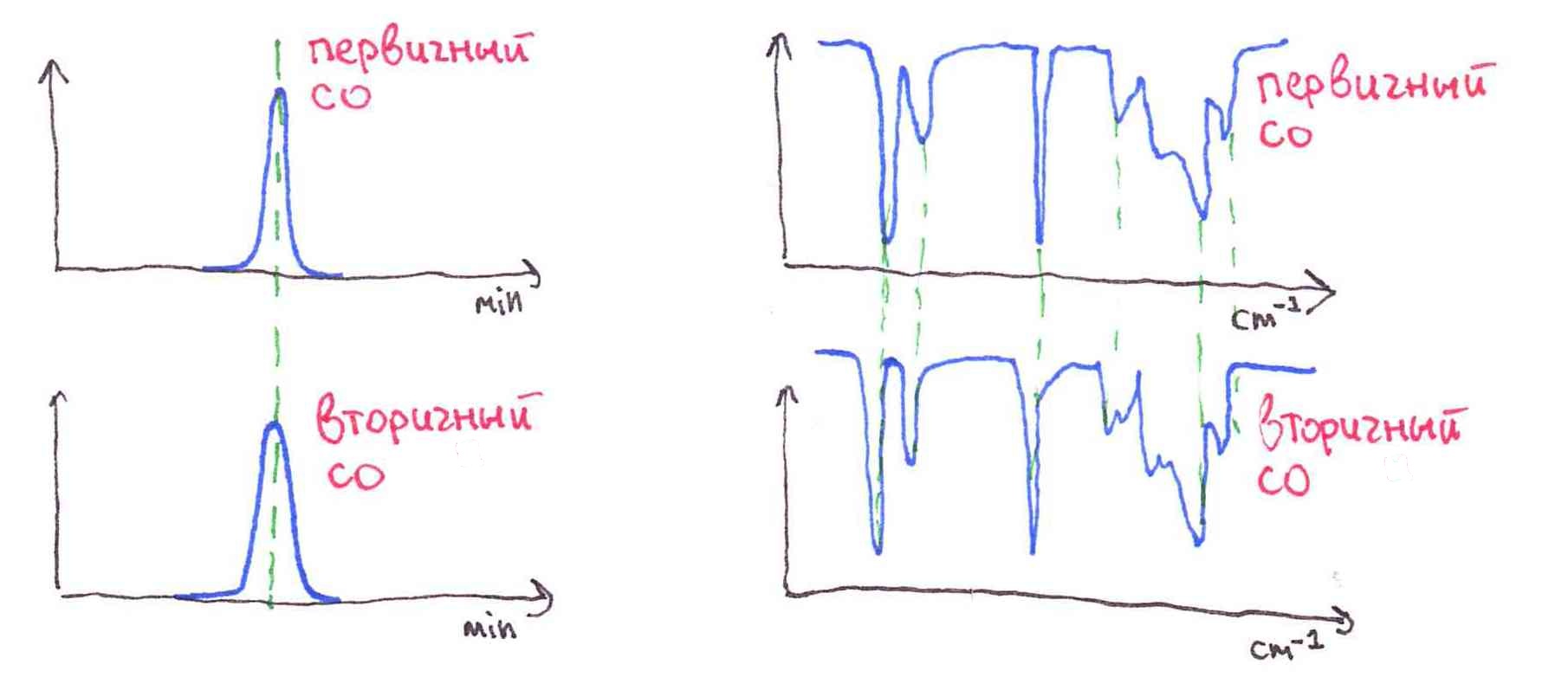
Подтверждение структуры вторичного (secondary) СО для качественного анализа проводят:
- по совпадению ИК-спектра с ИК-спектром первичного СО
- по совпадению времени удерживания на хроматограмме с временем удерживания первичного СО
Пример спецификации
СО основного вещества для количественного анализа
СО основного вещества для количественного анализа применяется:
- для приготовления раствора сравнения при количественном определении действующего вещества в препарате
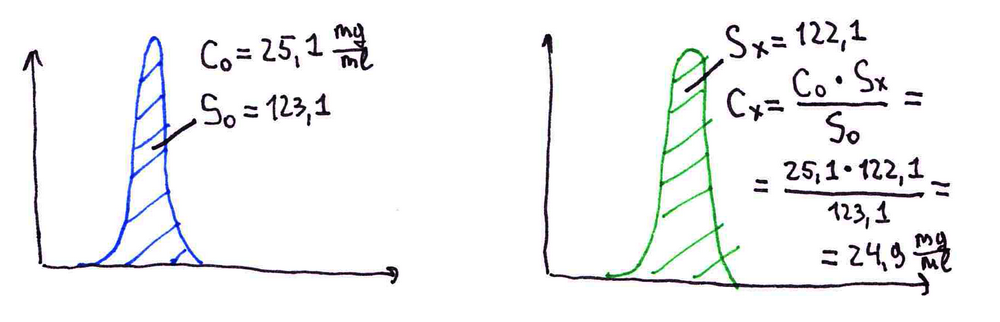
- для оценки правильности и линейности при валидации методики
- при контроле качества результатов анализа
Установление аттестованного значения для первичных СО
Аттестованных характеристики две - массовая доля основного вещества (МДОВ) и подлинность (структура).
Для первичных СО оба показателя должны устанавливаться первичными методам. Установление подлинности обсуждали в разделе про СО для качественно анализа.
К определению МДОВ в "СО для количественного определения" предъявляются особые требования. Считается необходимым подтвердить значение МДОВ как минимум двумя независимыми методами:
- Прямым титриметрическим методом (анализ должен проводиться по валидированной методике)
- Методом "баланса масс"
Для определения МДОВ методом "баланса масс":
- Проводят количественное определение примесей
Подразумевается, что определяют на просто "хроматографичесую частоту" на первой попавшейся ВЭЖХ-колонке, а проводят именно количественное определение примесей по методике, валидированной для данной субстанции (если требуется, с учетом относительных коэффициентов чувствительности) - Определяют потерю массы при высушивании (вода и органические растворители)
Если вещество нельзя нагревать - то определяют воду по Фишеру и остаточные методом ГХ. Остаточные растворители так же определяют отдельно и включают в расчет, если они не удаляются при 105оС или их содержание велико. - Оценивают содержание неорганических примесей (как правило, в виде сульфатной золы)
В расчетах это значение как правило не учитывают. - Рассчитывают содержание основного вещества
100% - сумма примесей - потеря массы при высушивании
Значение МДОВ, полученное прямым титриметрическим методом должно быть близко к значению, полученному методом "баланса масс".
Пример спецификации

Дополнительное подтверждение чистоты
В качестве дополнительного подтверждения чистоты используют элементный (CHNS)-анализ, дифференциальную сканирующую калориметрию (ДСК) и косвенно ЯМР.
CHNS-анализ
Существуют подход к расчету чистоту органических соединения по данным элементного анализа [Ревельский И.А. и др. Определение основного компонента в высокочистых химических веществах состояние вопроса и перспективы, Журн. аналит. хим., 2009, т. 64, № 9]. Однако, этот подход применим для высокочистых веществ, не содержащих примесей с теми же элементами, что и основное вещество. Для органических соединений и фарм. субстанций элементный анализ является скорее косвенным подтверждением структуры.
Дифференциальная сканирующая калориметрия
Если соединение и его примеси плавиться без разложения, описан подход к определению мольной доли примесей по ДСК-пику плавления [ASTM E928, USP <891>, ОФС 1.2.1.0027.18 "Термический анализ"]. Метод применим для ограниченного класса соединений.
Оценка наличия примесей по 1H-ЯМР спектру
При достаточно высоком содержании примесей (~ от 1 до 10%) они могут проявляться на 1H-ЯМР спектре в виде дополнительных пиков, не свойственных основному веществу.
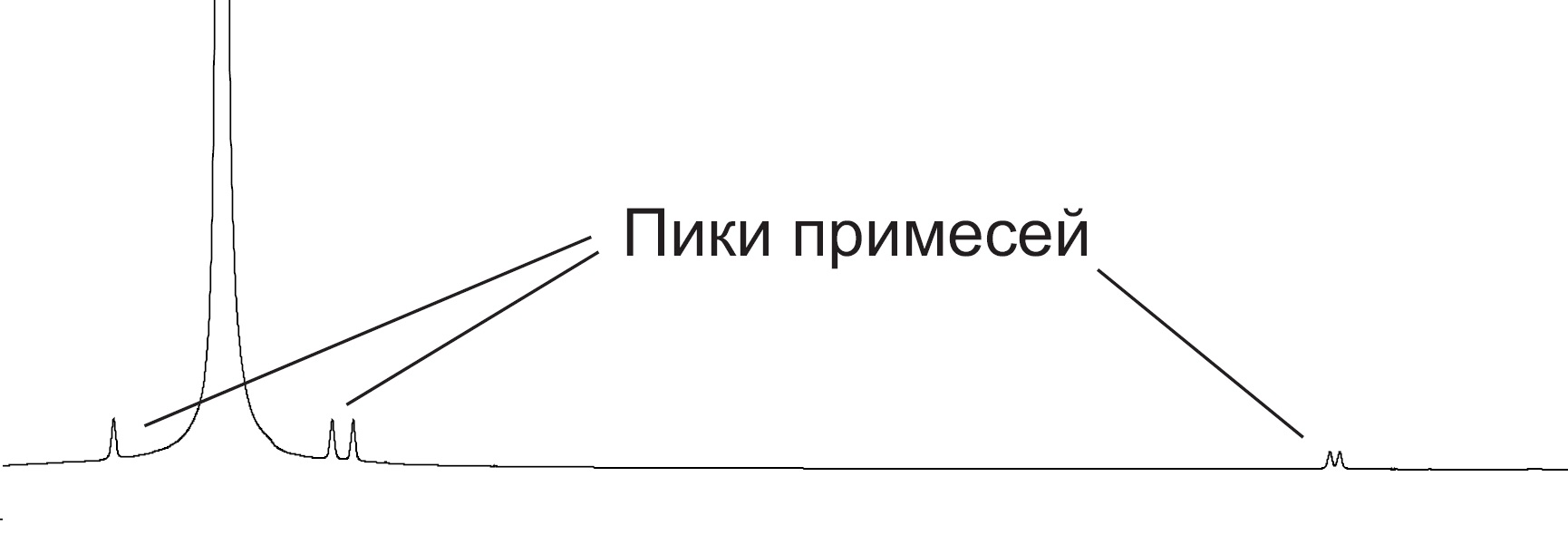
Результаты оценки чистоты методом CHNS-анализа, ДСК и ЯМР являются дополнительным косвенным подтверждением, и не используются в расчетах.
СО примесей
Для проверки разрешающей способности хроматографической системы достаточно использовать СО примеси для качественного анализа (без установления массовой доли основного вещества).
Если примесь не может быть получена в достаточном количестве, возможны следующие варианты:
- подготовка стандартного образца, содержащего смесь основного соединения(ий) и примеси или примесей;
- подготовка стандартного образца, содержащего смесь указанных примесей.
Для СО примесей для количественного анализа определяют структуру (подлинность) и массовую долю основного вещества (МДОВ). Требования к чистоте СО примесей ниже, чем для основного вещества:
При количественном содержании основного вещества от 95 % и выше его принимают за 100 %. При содержании основного вещества менее 95 % в расчетах необходимо учитывать значение фактического содержания.
Оценивание неопределенности аттестованного значения
Результаты определения аттестованного значения массовой доли основного вещества желательно представлять в виде:
(X ± U)%, где U - расширенная неопределенность результата измерений
 Пример паспорта стандартного образца (CRM): массовая доля основного вещества (99,2±0,2)%
Пример паспорта стандартного образца (CRM): массовая доля основного вещества (99,2±0,2)%
Существует два подхода к оценке неопределенности:
- На основе показателей прецизионности и правильности
согласно ИСО 21748 "Руководство по использованию оценок повторяемости, воспроизводимости и правильности при оценке неопределенности измерений" - Оценка неопределенности по составляющим
согласно руководству ЕВРАХИМ-СИТАК Quantifying Uncertainty in Analytical Measurement
Подробно об оценке неопределнности
Руководства, нормативные документы
Фармокопейный центр Украины и статья 5.12 ГФУ "Стандартные образцы" предьявляет особые требования к значению неопределенности СО:
Аттестация СО предприятия коренным образом отличается от обычного анализа субстанции на соответствие НД. Требования к неопределенности результатов для аттестации СО в 3 раза более жесткие (!), чем для анализа субстанции. В связи с этим при аттестации используются специальные приемы работы (поскольку фактически требования к результатам анализа близки к предельным возможностям метода анализа).
Аттестация, оценка однородности и стабильности, упаковка, маркировка и хранение
Аттестация СО предполагает проведение испытаний по исследованию однородности, стабильности, определению аттестованного значения и границ его погрешности или неопределенности, определению оптимальных условий хранения и транспортировки.
По итогам аттестации составляется отчет, содержащий следующие разделы:
- обоснование необходимости разработки и назначение СО
- описание технологии получения СО
- методика аттестации
- результаты аттестации
- оценка неопределенности аттестованного значения
- исследование стабильности СО
- исследование однородности СО
- копии свидетельств о поверке средств измерений
- сведения о валидации используемых методов
- проект паспорта на СО
- макет этикетки на СО
- инструкция по безопасному обращению с СО
Примеры оценки однородности и стабильности СО можно посмотреть в публикациях:
- Создание стандартного образца состава глицина (СГ СО УНИИМ) / М.П. Крашенинина [и др.] // Стандартные образцы. 2015. № 1. С. 23–33
- Разработка государственного вторичного эталона и стандартных образцов состава на основе жидкостной и газовой хроматографии / О.С. Шохина [и др.] // Стандартные образцы. 2017. Т. 13. № 1. С. 9–26. DOI 10.20915/2077-1177-2017-13-1-9-26
Где взять материал для изготовления СО предприятия?
СО основного вещества
- доочистить из субстанции
СО примеси
- купить примесь как "химическое вещество"
- заказать "синтез на заказ"
- выделить примесь из субстанции с помощью препаративной хроматографии
- использовать "субстанцию с примесями" без выделения
Где организовать аттестацию СО?
Для определения массовой доли основного вещества требуется валидированная титриметрическая методика, и валидированная методика количественного определения примесей (для "баланса масс").
Поэтому самым логичным решением является аттестация СО по показателю "массовая доля основного вещества" в заводской лаборатории предприятия, т.к. в ней уже внедрены валидированные методики анализа субстанции, из которой планируется делать СО.
Установление структуры СО первичными методами - спектроскопией ЯМР и масс-спектрометрией обычно заказывают в организации, имеющей соответствующее оборудование. Для аттестации потребуются актуальные свидетельства о поверке (т.к. они должны быть включены в отчет об аттестации).
Подтвердить структуру стандартного образца на поверенном оборудовании можно в нашей лаборатории.
Литература
- ОФС.1.1.0007.18 "Стандартные образцы", ГФ XIV
- Глава “Reference standards”, Handbook of isolation and characterization of impurities in pharmaceuticals, Academic Press, 2003
- Глава "Использование и аттестация стандартных образцов при контроле качества лекарственных средств", Валидация методик для производителей лекарств, пер. с нем. под. ред. В.В. Береговых, Москва, Литтера, 2008
- Кузьмина Н.Е. Возможности использования метода ЯМР при аттестации стандартных образцов, Стандартные образцы № 2, 2014
- Д.А. Леонтьев, Система вторичных стандартных образцов в лабораториях контроля качества лекарственных средств

